五月份承蒙倫敦臺灣生物醫學學會邀請,有機會參與第八屆跨領域生物醫學科學研討會(The 8th Interdisciplinary Biomedical Sciences Conference),當天特別從獼猴神經生理學的觀點切入,分享如何從了解大腦的電生理特徵,發展出治療大腦疾病的療法,以及獼猴神經生理研究如何與臨床研究相接軌,並且同時透過對正常大腦運作的了解,推動人工智慧演算法的革新。

神經生理學:神經系統的功能與運作
神經生理學(neurophysiology),主要在研究神經系統的「功能」以及其運作機制,而神經系統最主要的功能在感知內在生理狀態(interoception)和外在環境刺激(exteroception),並且產生適當的反應(肌肉收縮、腺體分泌等)。因此,神經系統的基本運作架構,必須要能夠進行傳遞訊息和處理訊息,以決定並執行輸出的反應。
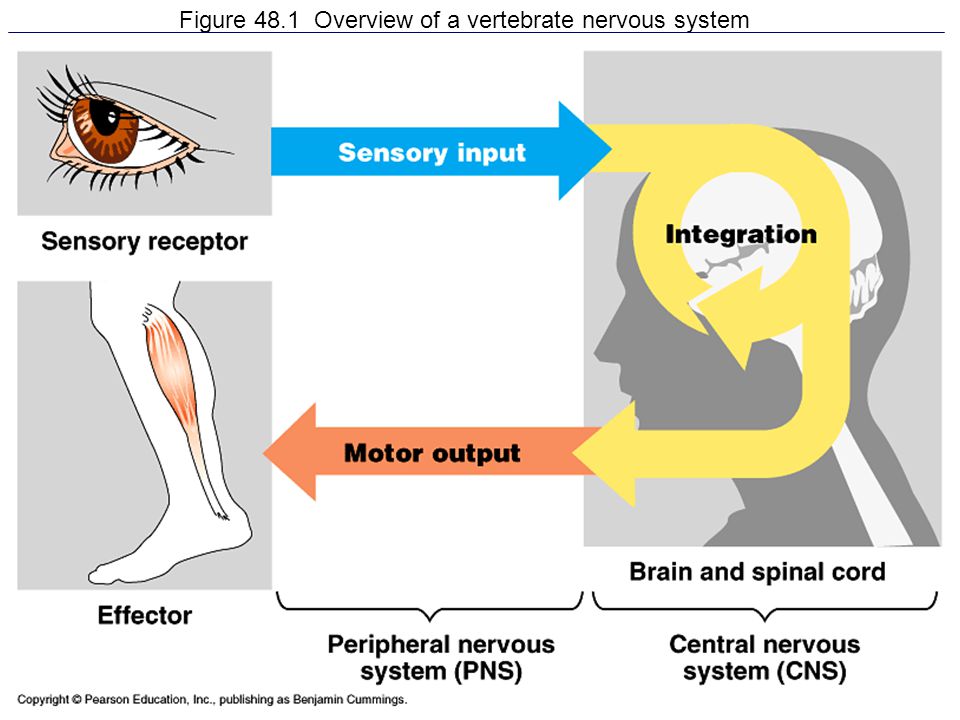
神經系統如何互相溝通:化學分子和電流訊號
神經系統由一個一個的神經細胞所串連組成,神經系統所處理的訊息,也由神經細胞構成的神經纖維,透過電流從細胞的一端傳送到另外一端。在兩個神經細胞交界處,稱為「突觸」(synapse),因為電流在此無法直接跨越細胞傳遞到下游,需要暫時把電流的能量轉換成成為稱為「神經傳導物質」(neurotransmitter)的化學分子,通過突觸的縫隙,擴散到對岸的細胞膜上。在下游神經細胞的表面,有特定的受體蛋白,可以感應這些不同的神經傳導物質,重新將化學訊號轉換成電流繼續傳遞下去。整個神經系統的訊號傳遞,就在化學分子和電訊號的不斷轉換當中,進行傳遞和訊號的整合。
大腦傳訊的一體兩面:化學訊號與電訊號
大腦中的化學訊息:神經傳導物質(neurotransmitter)
既然神經細胞之間透過各種的神經傳導物質來傳遞訊息,在每次訊號傳到突觸,轉化成化學訊號時,便提供我們人為調節迴路訊號的機會。透過外來的藥物調整異常的神經訊號,再讓它繼續往下游傳遞,便成為治療神經系統疾病的一種策略。然而單一神經元不一定只分泌一種神經傳導物質,同一神經傳導物質接觸到不同的受體,對下游神經元的影響也各自不同。因此,從化學分子的角度切入,了解神經迴路的運作,很難簡單地斷定特定神經傳導物質對大腦造成的影響。例如,當年叱詫風雲的百憂解(Prozac)主要的設計概念,是認為憂鬱症起因於腦中其中一種神經傳導物質--血清素(serotonin)不足,因此設計這類型的抗憂鬱藥物,使腦中的血清素增加。然而,經過這麼多年的研究和臨床使用,我們逐漸了解到,單純透過藥物增加腦中血清素後,大腦的受體會自己進行調節,其他神經傳導物質也會重新平衡,其影響是牽一髮而動全身,並不是缺甚麼補甚麼那麼簡單,其治療效果也因此無法像預期中那樣藥到病除。
大腦中的電流訊息:動作電位(action potential)
神經細胞在接收上游神經細胞傳送的訊息後,加以整合處理,如果訊號達到一定的條件,便會放出固定波形的「動作電位」(action potential)將訊息繼續往下傳送。這樣「全有全無」(all-or-none)的電路訊號就像是大腦中的摩斯密碼一樣,無時無刻都透過不同組合傳送著複雜的訊息,調控人體全身上下的運作。和化學分子不同,神經電訊號通常是局部的訊號,非常精準地指揮著下游的神經迴路。對於局部的神經迴路,目前也有各種不同的神經調節(neuromodulation)可以局部調整異常的神經迴路,讓整個大腦恢復運作。
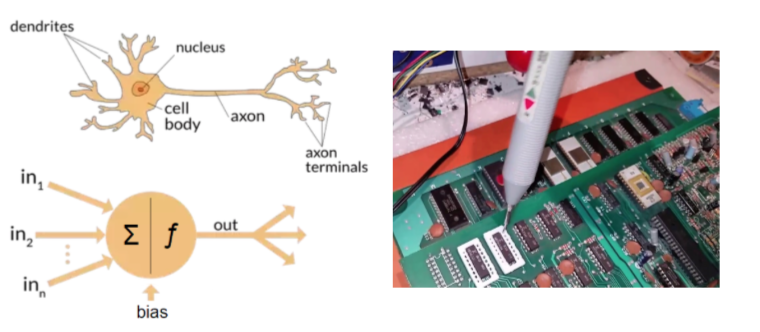
轉譯神經生理學(Translational Neurophysiology):治療異常的大腦傳訊
轉譯神經生理學,主要在應用我們對於大腦功能的了解,發展出神經疾病的嶄新治療方式。因此,基礎研究如何能應用在臨床治療上,與其研究切入的角度,以及現有的治療技術有關。舉例來說,如果研究找到可能造成失智症的化學分子,其臨床應用便是要發展抑制這種致病分子的藥物來進行治療。然而,使用藥物治療神經系統的疾病有許多困難和障礙。首先,藥物要進到大腦裡面需要通過一層大腦的保護層(血腦障壁,blood brain barrier, BBB),並不是所有藥物都有辦法到達大腦裡面。如果無法進入大腦,實驗室中效果再好的藥物也無法在人體作用。另外,藥物進到大腦以後擴散開來,對整個大腦都有所影響,無法只針對局部有問題的神經迴路進行調節。如果藥物把有問題的大腦區域治療好,但卻又影響到其他正常迴路的功能,治療的效果勢必不甚理想。
反之,電生理研究透過了解大腦電訊號的傳訊,如果發現了在特定疾病當中,大腦特定腦區會出現異常的電訊號,我們就可以利用植入電極的方式,另外給予大腦電流,來調節大腦原本的電訊號,達到治療疾病的效果。最有名的例子,便是已經廣泛使用在巴金森氏症患者身上的深部腦電刺激術(Deep Brain Stimulation, DBS),從1960年代在獼猴身上實驗成功,進行臨床試驗,到現在已經造福全球上百萬患者,臺灣的健保也從2015年原本只給付機器和一次電池的費用,到了2016年加碼給付終身電池費用,緊接著更即將在2019年8月進一步給付導線、導線延長線及導線固定蓋,造福更多患者。大腦電調節治療的發展速度比起傳統漫長的藥物臨床試驗快得許多,其立竿見影的療效也是藥物治療難以望其項背的,更重要的是, 電極所釋放的電流只會在電極局部有效果,不會像神經系統的藥物擴散到整個大腦裡頭,較能在矯正異常迴路時,保留其他腦區的運作 。
獼猴神經生理學 Primate Neurophysiology
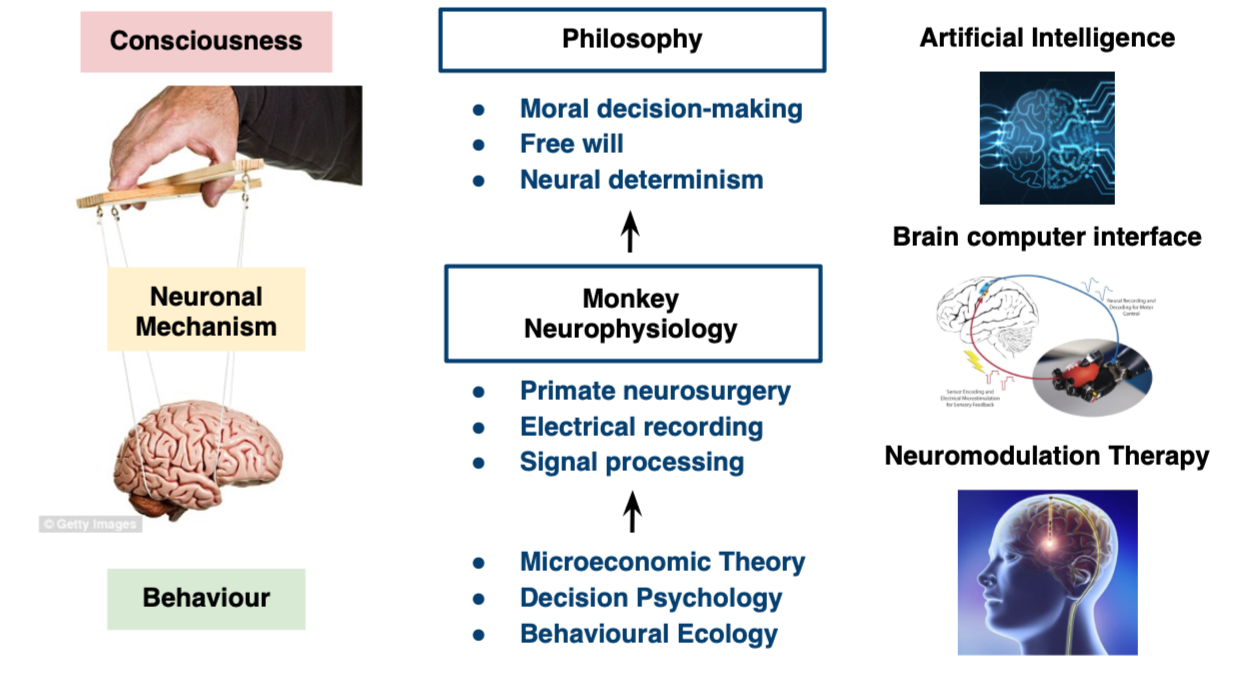
獼猴神經生理學,顧名思義是利用獼猴作為模式動物,研究神經系統的功能。使用獼猴的原因最主要的因素是獼猴的大腦結構和功能與人類十分相似,可以研究例如決策和社會互動等較為複雜的行為機制。 因此,獼猴神經生理學(primate decision neurophysiology)作為系統神經科學的「黃金準則」(golden standard),整合心理學、政治學、經濟學、行為生態學等領域對於個體行為的研究,進一部探討「行為」背後的神經機制。此大腦機制以及神經網路的運作模式,可應用在人工智慧演算法的發展,結合大腦訊號及先進的電機設計,更可以發展透過腦部訊號控制機械的腦機介面(Brain Computer Interface, BCI)。此外,腦科學關心人的行為,因此連結許多人文科學領域,對於人之所以為人的許多道德倫理議題,雖然無法直接回答,但腦神經科學家每天的工作,可以讓人反思科學象牙塔之外,人類社會的許多現象,也更增添科學研究的人文價值。
